
Šta dobre bakterije u crevima najviše „vole“, a šta im ne prija i utiče na imunitet, odgovara dr Đorđe Kralj
Crevni mikrobiom danas više ne posmatramo kao pasivnu skupinu mikroorganizama, već kao aktivnog partnera u regulaciji imuniteta, održavanju integriteta crevne barijere i oblikovanju metaboličkog zdravlja. Iako svest o mikrobiomu raste i menja se, još uvek je u građanstvu prisutno dosta nedoumica i fraza, koje nisu zasnovane na nauci. A ključ je: edukacija, pravilno informisanje i disciplina u prehrambenim navikama.
Imunitet nije „prekidač“ koji možemo samo da pojačamo
Šta nauka zaista zna o vezi mikrobioma i imunskog sistema, zašto su kratkolančane masne kiseline - posebno butirat - važne, kakvu ulogu imaju vlakna i mediteranski obrazac ishrane, i zbog čega je diverzitet ishrane jedan od najvažnijih praktičnih saveta za dugoročno očuvanje zdravlja creva, pitanja su na koja odgovara dr Đorđe Kralj, klinički lekar na specijalizaciji iz interne medicine (Klinika za interne bolesti KBC Zvezdara - Kliničko Odeljenje za gastroenterologiju i hepatologiju).
Čini se da šira javnost ranije nije bila informisana o povezanosti između crevne flore i imuniteta, a i danas se susrećemo sa instant rešenjima za brzo „podizanje“, odnosno takozvano „bustovanje“ snage imunskog sistema. Kako biste u najkraćem opisali ovu vezu očima nauke?
- Kada govorimo očima nauke, imunitet nije „prekidač“ koji možemo samo da pojačamo. Imunski sistem je složen regulatorni mehanizam čiji je cilj ravnoteža: da dovoljno snažno reaguje kada postoji infekcija ili opasnost, ali i da ne reaguje preterano, jer upravo tada nastaju hronična zapaljenja, alergije ili autoimune bolesti. U tom fino podešenom sistemu, crevni mikrobiom ima centralnu ulogu - objašnjava dr Kralj i precizira:
Cilj nije da imunitet bude „jači po svaku cenu“, već bolje regulisan
- Najveći deo imunološkog „dijaloga“ sa spoljnim svetom odvija se upravo na nivou creva. Mikroorganizmi koji tamo žive nisu pasivni putnici, već aktivni učesnici u sazrevanju i usmeravanju imunskog odgovora. Oni pomažu u održavanju zaštitne barijere, utiču na stvaranje zaštitne sluzi, učestvuju u nastanku brojnih metabolita i „uče“ imunski sistem toleranciji i pravilnoj proceni opasnosti. Posebno su važni metaboliti poznati kao kratkolančane masne kiseline, odnosno SCFA - acetat, propionat i butirat. Butirat je naročito značajan jer predstavlja glavni izvor energije za ćelije debelog creva, pomaže integritetu sluzokože i deluje protivupalno. Zato cilj nije da imunitet bude „jači po svaku cenu“, već bolje regulisan. U praksi to znači raznovrsna ishrana, dovoljan unos biljnih vlakana, manje ultra-prerađene hrane, dobar san, fizička aktivnost i racionalna upotreba antibiotika.
Znače li osetljiva creva obavezno i slabiji imunitet?
Creva su izdržljiva jer u njima završava sve ono što uđe u digestivni sistem, a sa druge strane kod nekih osoba su i veoma senzitivna. Da li one obavezno imaju i slabiji imunitet?
- Ne. Osetljiva creva ne znače automatski i slab imunitet. Osetljivost digestivnog sistema može biti posledica poremećene komunikacije između creva i nervnog sistema, promenjene pokretljivosti, visceralne preosetljivosti, prolazne postinfektivne neravnoteže ili promena u mikrobioti. Najbolji primer je sindrom iritabilnog creva, gde pacijent može imati izražene tegobe, a da pritom nema imunodeficijenciju. Tačnije je reći da kod nekih osoba postoji poremećena imunološka regulacija na nivou sluzokože ili narušen integritet crevne barijere, ali to nije isto što i globalno „slab“ imunitet. U mnogim stanjima problem nije u premalo imuniteta, već u tome što je imunski odgovor neadekvatno usmeren, pojačan ili loše koordinisan. Zato je uvek važno razlikovati funkcionalnu preosetljivost, organsko zapaljenje i pravu sistemsku imunološku slabost - precizira sagovornik eKlinika portala.
Posledice poremećene ravnoteže mikrobioma
Na pitanje koji su najčešći problemi i komplikacije kada se poremeti ravnoteža mikrobioma i dođe do disbioze, dr Đorđe Kralj odgovara da posledice mogu biti lokalne i sistemske. Prema njegovim rečima, prvi nivo problema nastaje u samim crevima: dolazi do smanjenja mikrobne raznovrsnosti, gubitka bakterija koje proizvode korisne metabolite i porasta mikroorganizama sa većim proinflamatornim potencijalom.
Doktor nam prenosi da se u mnogim studijama posebno izdvajaju smanjene količine vrsta kao što su Faecalibacterium prausnitzii, Roseburia intestinalis i drugi proizvođači butirata, dok određeni pripadnici porodice Enterobacteriaceae mogu biti zastupljeniji, i pojašnjava:
- To znači manju proizvodnju SCFA, slabiji epitelni integritet i veću propustljivost creva. Klinički, pacijent to može osećati kao nadimanje, bol, promene stolice, intoleranciju na pojedine namirnice i pojačanu sklonost hroničnom niskogradusnom zapaljenju. Dugoročno, disbioza se povezuje sa inflamatornim bolestima creva, infekcijom Clostridioides difficile, gojaznošću, insulinskom rezistencijom, metaboličkim poremećajima, masnom jetrom, ali i sa poremećajima na osi creva i mozga. Važno je naglasiti da ne postoji univerzalno pravilo da će isti probiotik pomoći svakom pacijentu. Efekti su soj-specifični, bolest-specifični i zavise od celokupnog okruženja u kome mikrobiota funkcioniše. Zato su u praksi najveći efekti najčešće rezultat dugoročne promene obrasca ishrane i životnih navika, a ne kratkotrajnih „detoks“ intervencija.
Brzi životni tempo i autoimune bolesti: Koji faktori još utiču na njihov razvoj?
Utisak je da svedočimo ekspanziji autoimunih bolesti. Koliko je za to zaslužan naš brzi način života koji obično podrazumeva i loše navike u ishrani?
- Brz način života i savremeni obrazac ishrane nisu jedini uzrok porasta autoimunih bolesti, ali jesu važan deo slagalice. Genetika daje podlogu, a životna sredina često odlučuje kako će se ta predispozicija ispoljiti. Hronični stres, nedostatak sna, sedentarni način života, pušenje, preterana upotreba antibiotika i ishrana bogata ultra-prerađenom hranom stvaraju okruženje koje pogoduje poremećaju mikrobioma, oštećenju barijere i produženoj imunološkoj aktivaciji. Posebno je problematičan zapadni obrazac ishrane - mnogo rafinisanih ugljenih hidrata, zasićenih masti, soli, aditiva i emulgatora, a malo biljnih vlakana i malo raznovrsne hrane. Takva ishrana je povezana sa manjom mikrobnom raznovrsnošću i manjom proizvodnjom protivupalnih metabolita. Nasuprot tome, mediteranski obrazac ishrane dosledno se povezuje sa povoljnijim profilom mikrobioma, boljom metaboličkom regulacijom i antiinflamatornim efektima. On podrazumeva mnogo povrća, voća, mahunarki, integralnih žitarica, maslinovog ulja, orašastih plodova, začinskog bilja i relativno malo ultra-prerađene hrane - detaljno objašnjava dr Đorđe Kralj.
Sojevi dobrih bakterija i najvažnije činjenice o vrstama vlakana
Šta je ono što dobre bakterije u crevima najviše „vole“, a šta im nikako ne pogoduje kada govorimo o ishrani?
- Dobre bakterije najviše „vole“ raznovrsnu biljnu hranu i različite tipove vlakana. To ne znači samo „više vlakana“, već više različitih vrsta vlakana. Nisu sva vlakna ista: postoje rastvorljiva i nerastvorljiva, fermentabilna i manje fermentabilna, viskozna i neviskozna. Među najvažnijim grupama su inulin i fruktooligosaharidi, galaktooligosaharidi, pektin, beta-glukani, arabinoksilani, psilijum, celuloza i rezistentni skrob. Na primer, inulin i FOS često podstiču rast bifidobakterija; rezistentni skrob predstavlja važan supstrat za vrste kao što je Ruminococcus bromii, a zatim posredno podržava i proizvođače butirata poput Eubacterium rectale i Roseburia; pektin iz voća mogu koristiti određene vrste roda Bacteroides; beta-glukani iz ovsa i ječma i vlakna iz integralnih žitarica takođe povećavaju stvaranje SCFA. U zdravom mikrobiomu posebno cenimo prisustvo vrsta kao što su Faecalibacterium prausnitzii, Roseburia intestinalis, Eubacterium rectale, Anaerobutyricum hallii i Akkermansia muciniphila - nabraja naš sagovornik.
Dodaje i da ono što mikrobioti nikako ne pogoduje jesu ultra-prerađena hrana, dugotrajno nizak unos vlakana, višak rafinisanog šećera, česta nepotrebna primena antibiotika i dugoročno jednostrana ishrana, ali naglašava da i dobra stvar može napraviti problem ako se uvede naglo: nagli porast fermentabilnih vlakana kod osoba sa osetljivim crevima može izazvati gasove, nadimanje i nelagodnost, pa zato, upozorava, povećanje treba da bude postepeno.

Mikrobiom i zapaljenske bolesti creva
Zapaljenske bolesti creva su posebno važan segment kliničkog i naučnog rada doktora Kralja i njegovih kolega pod okriljem IBD akademije. Koliko upalni procesi utiču na mikrobiom i šta je novo na polju naprednog lečenja ovih bolesti?
- Kod inflamatornih bolesti creva - pre svega Kronove bolesti i ulceroznog kolitisa - odnos između zapaljenja i mikrobioma je izrazito dvosmeran. Upala menja mikrookruženje u crevu: količinu kiseonika, sastav žučnih kiselina, dostupnost hranljivih materija, integritet sluzokože i lokalni imunitet. U takvim uslovima opada broj bakterija koje održavaju antiinflamatornu ravnotežu i proizvode butirat, a raste broj mikroorganizama koji bolje opstaju u zapaljenskoj sredini. Zbog toga kod IBD često nalazimo manju raznovrsnost mikrobioma, manje korisnih anaeroba kao što je Faecalibacterium prausnitzii, a više bakterija sa proinflamatornim potencijalom - navodi dr Đorđe Kralj.
Budućnost lečenja IBD i prekidanje začaranog kruga
Klinički lekar na specijalizaciji iz interne medicine slikovito opisuje da istovremeno i sama disbioza može dalje podsticati upalu, pa nastaje začarani krug.
- U lečenju IBD više nije cilj samo smirivanje simptoma, već dublja kontrola bolesti - biohemijska remisija, endoskopsko zarastanje, a kod odabranih pacijenata i još dublji oblici izlečenja sluzokože i zida creva. Pored anti-TNF lekova, anti-integrina i anti-IL-12/23 terapija, sve veći značaj imaju pristupi usmereni ka IL-23 osi, kao i male molekule poput JAK inhibitora i S1P modulatora. Istovremeno, raste interesovanje za mikrobiom-usmerene terapije - preciznije probiotske strategije, postbiotike, bakterijske metabolite i druge personalizovane pristupe - ali je to oblast koja se i dalje intenzivno razvija. Budućnost lečenja IBD sve više podrazumeva spoj imunologije, mikrobiologije, ishrane, biomarkera i personalizovane medicine - objasnio je u razgovoru za eKlinika portal dr Đorđe Kralj, čijom ljubaznošću vam prezentujemo i važan mini-vodič kroz svet vlakana u ishrani.
Praktični vodič za pacijente: Kako hraniti mikrobiom u svakodnevnom životu
Za većinu odraslih osoba realan i koristan cilj je najmanje 25 g vlakana dnevno, a u praksi se često preporučuje raspon od 25 do 30 g dnevno, uz postepeno povećanje i dovoljno tečnosti. Ključ nije samo u količini, već i u raznovrsnosti: različita vlakna hrane različite bakterije.
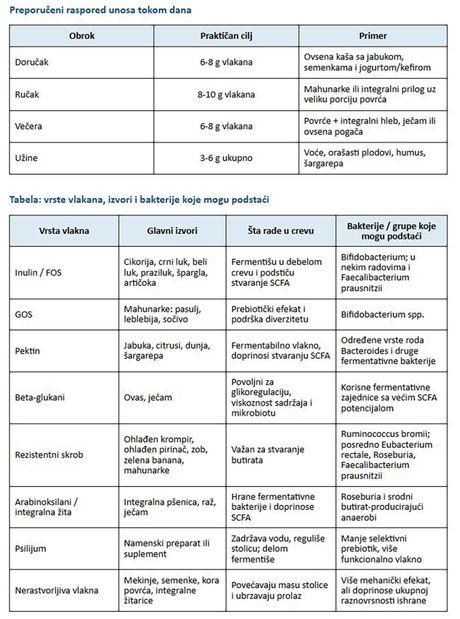
Napomene sagovornika eKlinika portala
Za praksu: povećanje unosa vlakana treba uvoditi postepeno, naročito kod osoba sa sindromom iritabilnog creva, izraženim nadimanjem ili aktivnom zapaljenskom bolešću creva. Ista vrsta vlakana ne prija svima jednako, pa je individualizacija važna koliko i sama preporuka.
Tekst je pisan u popularno-stručnom formatu i oslanja se na savremenu literaturu o mikrobiomu, kratkolančanim masnim kiselinama, mediteranskoj ishrani, vlaknima i savremenim pristupima u lečenju.
(eKlinika.rs)
eKlinika zadržava sva prava nad sadržajem. Za preuzimanje sadržaja pogledajte uputstva na stranici Uslovi korišćenja.



